Е.В. Федорова, Т.Л.
Семакова, Г.В. Ксенофонтова
Санкт-Петербургская
государственная химико-фармацевтическая академия
Синтез 5-арил-4,6-дихлор-5Н-пирано[2,3-d:6,5-d’]-дипиримидинов и их реакции с О- и
N-нуклеофильными агентами
Низкая
растворимость многих полученных ранее на кафедре органической химии СПХФА
5-арил-5Н-пирано[2,3-d:6,5-d’]дипиримидин-4,6-дионов
(Iа-в) в воде и большинстве органических растворителей
является существенным недостатком этих соединений при изучении их
физико-химических свойств и биологической активности. Введение в их молекулы
заместителей различной природы может повлиять как на липофильно-гидрофильные
свойства, так и на биологическую активность веществ, их транспорт и
биодоступность в организме.
Нами были
изучены реакции заместительного хлорирования 5-арил-5Н-пирано[2,3-d:6,5-d’]дипиримидин-4,6-дионов
(Iа-в) с последующим взаимодействием полученных продуктов с О-
и N-нуклеофильными агентами.
Дихлорпроизводные
(IIа-в) были получены при кипячении пирано-дипиримидинов (Iа-в)
в смеси РОС13 и РСl5 (Схема 1), при этом РСl5
брали
в трехкратном избытке на каждую гидроксильную группу пиранодипиримидинов (Iа-в).
Гидроксильные группы в положениях 4 и 6 пиранодипиримидинов (Iа-в) замещаются
хлором в течение 15-25 ч кипячения в РОС13 и РС15.
Выделяли дихлорпиранопиримидины (IIа-в) экстракцией
конечного продукта хлороформом из остатка, полученного при отгонке жидких
компонентов реакционной смеси. Предложенный способ выделения дихлорпроизводных
(IIа-в) позволяет избежать гидролиза дихлорпиранодипиримидинов
(IIа-в) и получать их чистыми и с высоким выходом. Выходы
продуктов заместительного хлорирования (IIа-в) составили от 86% до
количественного.
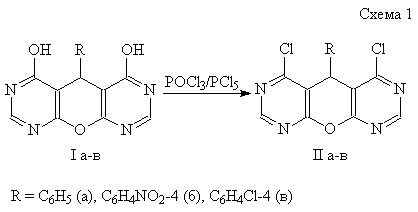
Дихлорпиранодипиримидины
(IIа-в) реагируют с О-нуклеофильными реагентами с образованием
4,6-диалкоксипиранодипиримидинов (IIIа-в) и
N-нуклеофилами
с образованием 4,6-диамино(диариламино-, дигидразино-)-пиранодипиримидинов (IV – VI а-в)
(Схема 2).
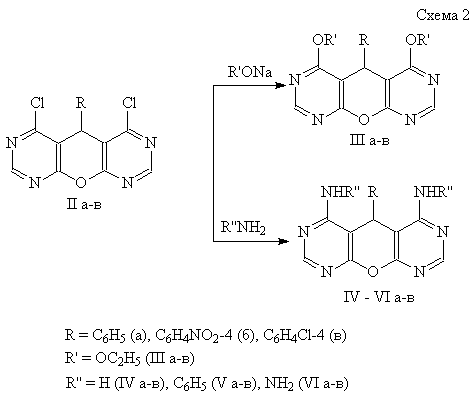
Реакции
нуклеофильного замещения проводили в спиртах и диоксане в зависимости от выбора
нуклеофильного агента при 40-50°С, выходы продуктов нуклеофильного замещения
составили от 64% до количественного. Дихлорпроизводные (IIа-в)
легко реагируют с этилатом натрия, аммиаком и первичными аминами, переход к
ароматическим аминам затрудняет нуклеофильное замещение у С4 и С6
дихлорпиранодипиримидинов (IIа-в), что сказывается на
условиях протекания (время выдержки от 2 до 10 ч) и выходах конечных продуктов
нуклеофильного замещения (III – VI
а-в).
Таким
образом, разработан удобный метод получения дихлорпиранодипиримидинов (II)
с высоким выходом и чистотой. Дихлорпроизводные (II) легко взаимодействуют с
О- и N-нуклеофилами с образованием
4,6-диалкоксипиранодипиримидинов (III) и
4,6-диамино-(диариламино-, дигидразино-)пиранодипиримидинов (IV –
VI).
Строение
полученных веществ (V-IX) доказано методами ЯМР 1Н
и 13С, УФ, ИК спектроскопии, индивидуальность – методом ТСХ, состав
– методом элементного анализа.