УДК 620.193
АНОДНОЕ ПОВЕДЕНИЕ СПЛАВОВ СИСТЕМ
Zn5Al-Mg и Zn55Al-Mg, В НЕЙТРАЛЬНОЙ
СРЕДЕ NaCI
З.Р. Обидов, И.Н. Ганиев, А.Н. Резо, Н.И. Ганиева
Институт химии им. В.И. Никитина АН
Республики Таджикистан, Душанбе
Приведены результаты исследования анодного
поведения сплавов Zn5Al, Zn55Al, легированных магнием, в среде электролита NaCI.
Проведённые потенциодинамические исследования цинк-алюминиевых сплавов, легированного магнием позволяют получить коррозионностойкие покрытия с
оптимальной концентрацией магния 0.005–0.1 мас.%. Скорость коррозии данных
сплавов в 2–2.5 раза ниже, чем исходных сплавов Zn5Al, Zn55Al и они могут использоваться в
качестве антикоррозионного покрытия для защиты от коррозии стальных сооружений.
Ключевые слова: цинк-алюминиевый сплав –
коррозионно-электрохимические свойства – потенциодинамический метод – анодное поведение – магний.
В связи с синтезом новых сплавов и внедрением их в
технику, а также расширением масштаба применения цинка, алюминия и сплавов на
их основе, особенно в агрессивных
средах, вопросы улучшения коррозионной стойкости становятся актуальными [1].
Работа посвящена исследованию влияния добавок магния на анодное поведение сплавов Zn5Al (5 мас.%
алюминия) и Zn55Al (55 мас.% алюминия), предназначенного
для нанесения защитных покрытий горячим методом.
Методики эксперимента
В качестве исходного
материала использовали алюминий марки А7, цинк марки ч.д.а., гранулированный и магний металлический – гранулированный марки х.ч. Из указанных металлов были получены сплавы в тиглях
из оксида алюминия в шахтной
печи сопротивления типа СШОЛ в интервале температур 750–850
°С. Сплавы отливали в графитовой изложнице,
диаметром 8 и длиной 140 мм. Нерабочая часть образцов изолировалась смолой (смесь 50% канифоли и 50%
парафина). Рабочую торцевую часть зачищали наждачной бумагой, полировали, обезжиривали, травили в 10%-ном
растворе NaOH,
тщательно промывали спиртом и затем погружали
в раствор NaCI. Температура раствора в ячейке поддерживалась
постоянная (20 0С) с помощью термостата МLШ–8. Электродом
сравнения служил насыщенный хлорсеребряный, вспомогательным – платиновый.
Исследование анодного
поведения сплавов Zn5Al, Zn55Al, легированного магнием
проводилось в электролитах NaCl с концентрациями 0.03;
0.3 и 3% на потенциостате ПИ–50.1.1 со скоростью развёртки потенциала 2 мВ/сек по методике, описанной в работе [2]. При электрохимических исследованиях образцы потенциодинамически
анодно поляризовали от бестокового потенциала, установившегося при погружении,
до резкого возрастания тока в результате питтингообразования. Затем образцы
поляризовали в обратном направлении до потенциала – 1400 мВ, в результате чего
происходило подщелачивание приэлектродного слоя. Наконец, образцы поляризовали
вновь в положительном направлении. Экстраполяция катодных кривых проводилось до
потенциала -1.600 ¸ -1.800 В. Плотности тока коррозии как основной
электрохимической характеристики
процесса коррозии, определяли по катодной кривой с учётом наклона тафелевской
прямой, равной bк = 0.124 В [3]. В
качестве примера на рис. 1 представлена потенциодинамическая поляризационная
кривая сплава Zn55Al, легированного 0.05 мас.% магнием. Расчёт плотности тока коррозии
(i, А/м2) проводили по следующим
уравнениям:
S = πr2 ; i = I / S ,
где S – рабочая поверхность круглых образцов, м2; I – сила
тока коррозии, А.
Скорость коррозии в свою очередь является
функцией тока коррозии, находимой по
формуле:
K = iкорр. .
к ,
где: к – электрохимический эквивалент, численное значение, которого для цинка
составляет 1.22 (для сплава Zn5Al) и 0.778 г/А∙ч как
усреднённое для цинка (1.22) и алюминия (0.335) для сплава Zn55Al,
которое на половине состоит из алюминия.
Экспериментальная
часть
Приведенные
на рис. 2 изменение потенциала коррозии сплава Zn5Al,
легированного магнием во времени в среде электролита 3%-ного NaCl фиксировалось в течение часа, который показывает, что
впервые минуты погружения сплава в раствор происходит резкое смещение
потенциала в положительную область. Как видно, по мере увеличении концентрации
хлор-ионов в электролите потенциал коррозии (-Екор) уменьшается, что свидетельствует о
понижении коррозионной стойкости сплавов в среде NaCl.
Результаты
исследования анодного поведения сплавов Zn5Al и Zn55Al,
легированного магнием, представленные в табл. 1 и 2, свидетельствуют, что
добавки магния в пределах 0.005–0.1 мас.% сдвигают
потенциал коррозии исходных сплава сплавов Zn5Al и Zn55Al в положительную сторону. Однако дальнейший рост
содержания магния в сплавах до 2.0 мас.%
сдвигает Екор в отрицательную
область и при этом наиболее заметен и сдвиг потенциала питтингообразования (Еno) и репассивации (Ерп)
в отрицательном направлении. Вышеперечисленная особенность наблюдалось в трех
исследованных средах.
Как
видно из табл. 1 и 2, с увеличением концентрации хлор–ионов потенциалы коррозии, питтингообразования и скорость коррозии сплавов
Zn5Al и Zn55Al, легированных
магнием уменьшаются, что указывает на снижение коррозионной стойкости сплавов
под воздействием хлор–ионов. Таким образом, сплавы легированные магнием
характеризуются более низким значением скорости коррозии, чем исходных цинк-алюминиевых
сплавов (табл. 1, 2).
В
целом, проведённые электрохимические исследования цинк-алюминиевых сплавов Zn5Al и Zn55Al, легированного магнием позволяют получить
коррозионностойкие покрытия с оптимальной концентрацией магния 0.005–0.1 мас.%. Скорость коррозии данных сплавов в 2–2.5 раза ниже, чем исходного сплава и они могут использоваться в качестве
анодного покрытия для защиты от коррозии стальных сооружений.
Выводы
Установлены
закономерности изменения электрохимических характеристик сплавов Zn5Al и Zn55Al, легированных магнием, в растворах NaCl с концентрациями
0.03, 0.3 и 3%. В частности показано, что
увеличение концентрации хлор-ионов в электролите способствует уменьшению
величины потенциала коррозии. Определено, что потенциалы
питтингообразования и репассивации с ростом концентрации легирующего элемента в сплавах смещаются в положительную, а с
увеличением концентрации хлор–ионов в растворе
в отрицательную область. Скорость коррозии исходных
сплавов Zn5Al и Zn55Al уменьшается в 2–2.5 раза при легировании их магнием до 0.1%.
Список
литературы
1. Фрейман
Л.И., Макаров В.А., Брыксин И.Е. Потенциостатические
методы в коррозионных
исследованиях и электрохимической защите. Под ред. акад. Я.М. Колотыркина. Л.: Химия,
1972. 240 с.
2.
Умарова Т.М., Ганиев И.Н. Коррозия
двойных алюминиевых сплавов в
нейтральных
средах. Душанбе: Дониш, 2007. 258 с.
3. Колотыркина Я.М. Металл и коррозия. М.: Металлургия, 1985. 88 с.
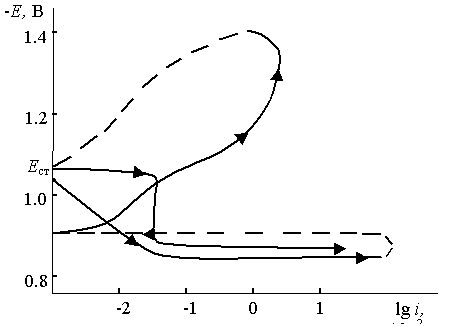
Рис. 1. Потенциодинамическая поляризационная кривая сплава Zn55Al,
содержащего
0.05 мас.% магния в 3%-ном растворе NaCl.
Е – потенциал (В), i - плотности тока (А∙м-2).
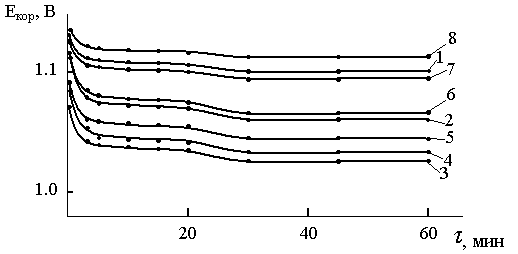
Рис.
2. Изменение потенциала свободной коррозии
Екор (В) во времени
τ (мин) сплавов Zn5Al (1), содержащих магний (2-8) в среде
электролита 3%-ного NaCl. СMg (мас.%):
2 – 0.005, 3 – 0.01,
4 – 0.05, 5 – 0.1, 6 – 0.5, 7–1.0, 8–2.0.
Таблица 1
Коррозионно-электрохимические характеристики сплава Zn5Al,
легированного магнием, в среде электролита NaCl
|
Среда |
Содер-жание магния в
сплаве, мас.% |
Электрохимические свойства
|
Скорость коррозии |
|||||
|
-Есв.корр. |
-Екорр. |
-Епо. |
-Ереп. |
iкорр.∙10-2 |
K∙10-3 |
|||
В
|
А/м2 |
г/м2 ∙ ч |
||||||
|
0.03% NaCI |
-
|
1.050 |
1.060 |
0.915 |
0.930 |
0.102 |
1.24 |
|
0.005
|
0.998 |
1.000 |
0.845 |
0.922 |
0.031 |
0.38 |
||
0.01
|
0.969 |
0.972 |
0.825 |
0.958 |
0.026 |
0.32 |
||
0.05
|
0.977 |
0.980 |
0.855 |
0.962 |
0.033 |
0.40 |
||
0.1
|
0.985 |
0.987 |
0.870 |
0.970 |
0.034 |
0.41 |
||
0.5
|
1.005 |
1.010 |
0.895 |
0.982 |
0.041 |
0.50 |
||
1.0
|
1.020 |
1.025 |
0.910 |
0.988 |
0.059 |
0.72 |
||
2.0
|
1.055 |
1.060 |
0.925 |
0.995 |
0.068 |
0.83 |
||
|
0.3% NaCI |
-
|
1.070 |
1.080 |
0.935 |
0.950 |
0.105 |
1.28 |
|
0.005
|
1.014 |
1.022 |
0.880 |
0.942 |
0.033 |
0.40 |
||
0.01
|
0.976 |
0.983 |
0.905 |
0.963 |
0.029 |
0.35 |
||
0.05
|
0.980 |
0.990 |
0.912 |
0.968 |
0.036 |
0.44 |
||
0.1
|
0.997 |
1.000 |
0.924 |
0.974 |
0.037 |
0.45 |
||
0.5
|
1.018 |
1.017 |
0.930 |
0.980 |
0.045 |
0.55 |
||
1.0
|
1.040 |
1.045 |
0.935 |
0.985 |
0.064 |
0.78 |
||
2.0
|
1.075 |
1.075 |
0.940 |
0.990 |
0.076 |
0.93 |
||
|
3% NaCI |
-
|
1.100 |
1.115 |
0.965 |
0.980 |
0.109 |
1.33 |
|
0.005
|
1.060 |
1.065 |
0.915 |
0.955 |
0.037 |
0.45 |
||
0.01
|
1.025 |
1.030 |
0.908 |
0.945 |
0.032 |
0.39 |
||
0.05
|
1.032 |
1.038 |
0.920 |
0.950 |
0.039 |
0.47 |
||
0.1
|
1.042 |
1.045 |
0.933 |
0.962 |
0.040 |
0.48 |
||
0.5
|
1.064 |
1.065 |
0.944 |
0.970 |
0.053 |
0.65 |
||
1.0
|
1.095 |
1.100 |
0.975 |
0.985 |
0.071 |
0.86 |
||
2.0
|
1.112 |
1.115 |
0.983 |
1.000 |
0.080 |
0.97 |
||
Таблица 2
Коррозионно-электрохимические характеристики сплава Zn55Al,
легированного магнием, в среде электролита NaCl
|
Среда |
Содер-жание магния в
сплаве, мас.% |
Электрохимические свойства
|
Скорость коррозии |
|||||
|
-Есв.корр. |
-Екорр. |
-Епо. |
-Ереп. |
iкорр.∙10-2 |
K∙10-3 |
|||
В
|
А/м2 |
г/м2 ∙ ч |
||||||
|
0.03% NaCI |
-
|
0.970 |
0.990 |
0.850 |
0.870 |
0.030 |
0.233 |
|
0.005
|
0.920 |
0.930 |
0.815 |
0.835 |
0.010 |
0.078 |
||
0.01
|
0.950 |
0.960 |
0.822 |
0.866 |
0.007 |
0.054 |
||
0.05
|
0.956 |
0.973 |
0.835 |
0.870 |
0.006 |
0.047 |
||
0.1
|
0.972 |
0.980 |
0.848 |
0.880 |
0.012 |
0.093 |
||
0.5
|
0.980 |
0.990 |
0.880 |
0.890 |
0.016 |
0.124 |
||
1.0
|
1.005 |
1.012 |
0.895 |
0.902 |
0.021 |
0.163 |
||
2.0
|
1.033 |
1.045 |
0.900 |
0.914 |
0.027 |
0.210 |
||
|
0.3% NaCI |
-
|
1.000 |
1.020 |
0.880 |
0.890 |
0.033 |
0.257 |
|
0.005
|
0.995 |
1.005 |
0.820 |
0.860 |
0.012 |
0.093 |
||
0.01
|
1.018 |
1.023 |
0.843 |
0.880 |
0.008 |
0.062 |
||
0.05
|
1.024 |
1.035 |
0.860 |
0.875 |
0.007 |
0.054 |
||
0.1
|
1.040 |
1.055 |
0.875 |
0.885 |
0.014 |
0.109 |
||
0.5
|
1.063 |
1.066 |
0.935 |
0.950 |
0.017 |
0.132 |
||
1.0
|
1.075 |
1.081 |
0.952 |
0.965 |
0.024 |
0.187 |
||
2.0
|
1.080 |
1.090 |
0.960 |
0.976 |
0.031 |
0.241 |
||
|
3% NaCI |
-
|
1.020 |
1.040 |
0.900 |
0.920 |
0.037 |
0.288 |
|
0.005
|
1.010 |
1.015 |
0.845 |
0.880 |
0.015 |
0.117 |
||
0.01
|
1.022 |
1.032 |
0.866 |
0.930 |
0.009 |
0.070 |
||
0.05
|
1.030 |
1.045 |
0.870 |
0.930 |
0.013 |
0.101 |
||
0.1
|
1.048 |
1.064 |
0.883 |
0.951 |
0.015 |
0.117 |
||
0.5
|
1.069 |
1.078 |
0.950 |
0.979 |
0.025 |
0.195 |
||
1.0
|
1.120 |
1.133 |
0.967 |
0.992 |
0.030 |
0.233 |
||
2.0
|
1.165 |
1.172 |
0.983 |
0.105 |
0.036 |
0.280 |
||
СВЕДЕНИЯ
об авторах
|
№ |
Ф.И.О. |
Должность, уч. степень |
Домашний адрес и тел. |
|
1 |
Ганиев Изатулло Наврузович |
Зав. лабораторией
Института химии АН РТ,
академик АН Республики Таджикистан, д.х.н., профессор |
Республика Таджикистан, г.Душанбе, пр. А.Сино,
734043, дом 130/5-49 |
|
2 |
Обидов Зиёдулло Рахматович |
К.т.н.,
старший научный сотрудник лаборатории
«Коррозионностойкие материалы» Института
химии АН РТ |
Республика Таджикистан, г.Душанбе,
пр. Борбад, 734061, дом 48/28-209 тел.: 934218210 E-mail: z.r.obidov@mail.ru |
|
3 |
Амини
Резо Наджафабади |
Аспирант Института
химии АН Республики Таджикистан |
Республика Таджикистан, г.Душанбе, пр. Борбад, 734061, дом 46/31-99 |
|
4 |
Ганиева Наргис Изатуллоевна |
К.т.н., доцент ТТУ им. акад.
М.С. Осими |
Республика Таджикистан. г.Душанбе, пр. А.Сино, 734043, дом 130/6-15 |