Обсуждение
результатов.
Общий анализ
экспериментальных результатов показывает, что содержание свинца в исходном штейне
на оксидную растворимость меди оказывает лишь слабое влияние. В случае со
свинцом, его растворимость в шлаке определяется как изменением отношения Cu/Pb, так и
содержанием железа в штейне. В результате совместной математической обработки экспериментальных
и промышленных данных получены следующие уравнения:
(Cu) = 0,199 + 3,118*10ˉ³[Cu] – 2,29*10ˉ³[Pb], r = 0,92;
(1)
(Pb) = 0,431 + 0,011[Pb] – 1,127*10ˉ³[Fe] ,
r = 0,94.
(2)
где
r – коэффициент корреляции.
Высокое значение коэффициентов
корреляции r = 0,92 и r = 0,94 свидетельствует о сильной связи между рассматриваемыми
величинами. Нетрудно видеть, что растворимость свинца в шлаке падает с
повышением содержания железа в штейне. Установленная количественная зависимость
подтверждает оксидный механизм перехода свинца в шлак.
Для
более точного прогнозирования растворимости меди и свинца в шлаке нами построены
уравнения множественной корреляции, описывающие зависимость искомых величин от
состава штейна. Полученные уравнения имеют следующий вид:
(Cu) = – 9,819 + 0,128 [Cu] + 0,113 [Pb] +
0,167 [Fe], r = 0,97; (3)
(Pb) = 5,734 – 0,07 [Сu] – 0,05 [Pb] – 0,09 [Fe], r =
0,98, (4)
где
r – коэффициент множественной корреляции.
Уравнения
(1) – (4) позволяют оценить влияние состава штейна на конечное содержание меди
и свинца в шлаке и могут быть использованы для количественной оценки растворенных
потерь металлов со шлаком на практике.
На следующем этапе
исследований определяли коэффициент распределения металлов, который представлял
традиционную задачу расчета исходя из отношения содержания металла в штейне к
его содержанию в шлаке. Результаты рассчитанных значений коэффициента
распределения меди, свинца, мышьяка и сурьмы сведены в таблицу.
На рис.1-4 показаны
зависимости коэффициентов распределения металлов между штейном и шлаком от их
содержания в штейне при постоянном значении давления кислорода и серы, а также
температуры. Нетрудно видеть общую закономерность для меди и мышьяка –
коэффициенты распределения повышаются с увеличением их содержания в штейне (рис.2,
4). Результаты по коэффициенту распределения этих металлов практически ложатся
на прямую линию, при незначительном разбросе данных. Это свидетельствует о том,
что в рассматриваемой системе механизм перехода меди и мышьяка в шлак описывается реакциями их окисления. При этом их потери
со шлаком определяются оксидной формой растворимости в шлаках.
Обращает на себя
внимание то, что коэффициент распределения свинца между штейном и шлаком плавно
снижается с увеличением содержания свинца в штейне. Причем при низких концентрациях
свинца наблюдается заметный разброс данных (рис.1).
Коэффициент распределения сурьмы с
увеличением ее содержания в штейне меняется слабо, и находится практически на
одном уровне (рис.3). Данное положение согласуется с выводами работы [3], где установлено,
что в условиях восстановительной атмосферы переход сурьмы из штейна в шлак в
основном обуславливается его переходом в шлак в виде Sb0.
Наблюдаемые на рис.1-4
зависимости неплохо описываются уравнениями, построенными в результате
математической обработки экспериментальных данных, которые имеют вид:
LCu / 10 = 0,93 + 0,37 [Cu], r = 0,91; (5)
LPb = 45,23 – 0,69 [Pb], r = 0,77; (6)
LAs = 1,44 + 2,88 [As], r
= 0,89; (7)
LSb = 2,96 + 0,74 [Sb], r = 0,74, (8)
где r – коэффициент парной корреляции.
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
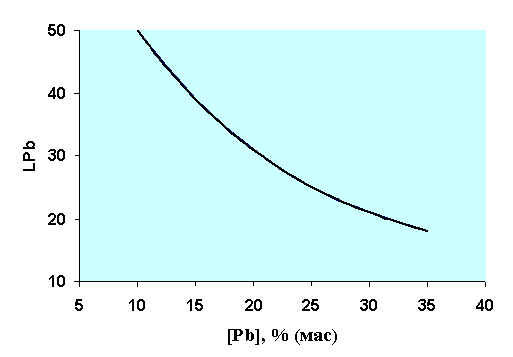
Рис.1.
Зависимость коэффициента распределения свинца (LPb)
от его содержания в штейне, % (мас.)
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
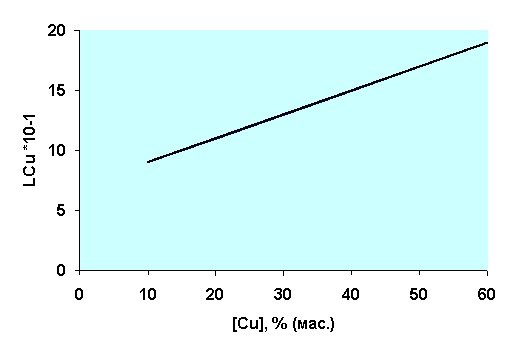
Рис.2.
Зависимость коэффициента распределения меди (LCu*10-1)
от ее содержания в штейне, % (мас.)
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
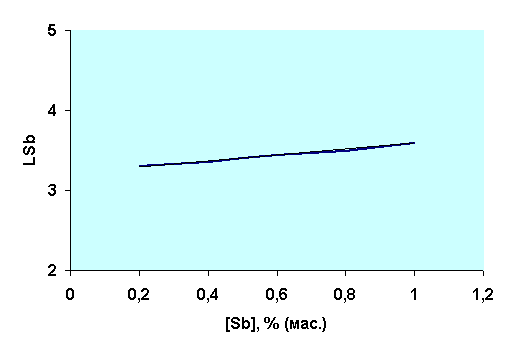
Рис.3.
Зависимость коэффициента распределения сурьмы (LSb)
от его содержания в штейне, % (мас.)

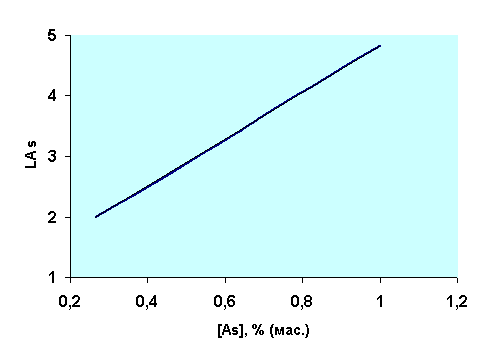
Рис.4.
Зависимость коэффициента распределения мышьяка (LAs)
от его содержания в штейне, % (мас.)
Сравнительно высокие коэффициенты
корреляции уравнений (5) и (7) указывают на сильную связь между
рассматриваемыми величинами.
Коэффициенты корреляции уравнений (6) и (8)
также указывают на сильную связь величин между собой. Относительно низкое
значение коэффициента корреляции уравнения (8) для сурьмы объясняется
спецификой механизма перехода сурьмы из штейна в шлак – в металлической форме.
Уравнение (6) описывает зависимость
коэффициента распределения свинца для всего массива без учета отношения Cu/Pb. В тоже время
установлено, что содержание растворенного свинца в шлаке существенно снижается
при увеличении данного отношения. По-видимому, при учете отношения Cu/Pb можно было бы
построить более точное уравнение. Обратный знак перед значением содержания
свинца в штейне, полученное в уравнении (6) подтверждает направление кривой,
показанной на рис.1.
Установленные
закономерности для свинца подтверждают сложный механизм его перехода в шлак. В
условиях опытов термодинамическая вероятность окисления сульфида свинца
возможна по реакциям:
[PbS] + 3/2O2 = (PbO) + SO2, (9)
[PbS] + (FeO) = (PbO) + [FeS]. (10)
Протекание реакции (9)
предпочтительнее (ΔG = −290552,2
Дж/моль), чем протекание реакции (10), для которой энергия Гиббса составляет
ΔG = – 85372 Дж/моль.
При равновесии системы
константы этих реакций равны между собой. Следовательно, можно записать:
a(PbO)*PSO2 / a[PbS]*PO2³/²
= a(PbO)*a[FeS] / a[PbS]*a(FeO). (11)
Учитывая, что в
условиях опытов величины РО2 и РSО2
фиксированы решим левую часть выражения (11) относительно a(PbO):
N(PbO) = K1* N[PbS], (12)
где - a(PbO) и a[PbS] заменено
на произведение N(PbO) *γ(PbO) и N[PbS]* γ(PbS) ;
К1 – постоянная величина, К1 =
К(9)*РО2* γ[PbS] / PSO2* γ(PbO).
С другой стороны,
решение правой части выражения (11) относительно a(PbO) позволяет записать:
N(PbO)
= K2* N[PbS] / N[FeS], (13)
где -
активности заменены на произведение N*γ;
К2 = К(10)* γ[PbS]*N(FeO)* γ(FeO) / γ [FeS]* γ(PbO).
Из выражения (13) нетрудно видеть, что
отношение NPbS / NPbO ≈ LPb обратно
пропорционально содержанию железа в штейне - NFeS. При увеличении содержания свинца в штейне содержание
железа в нем уменьшается, что в свою очередь ведет к снижению коэффициента
распределения свинца между штейном и шлаком. Обратный характер зависимости
коэффициента распределения свинца от его содержания в штейне, показанный на рис.1,
полностью подтверждает это положение.
Совместный анализ
экспериментальных и промышленных результатов позволяет сделать ряд обобщающих
выводов. В восстановительных условиях растворимость меди в шлаках, как в
условиях эксперимента, так и в промышленных условиях определяется содержанием
сульфида меди в штейне. Напомним, что в промышленных штейнах около 80 % меди,
от общего ее содержания, присутствует в
сульфидной форме. При этом механизм перехода меди из штей-на в шлак
подчиняется традиционным закономерностям и определяется в основном оксидной ее
растворимостью.
В случае со свинцом картина представляется
более сложной. В промышленных штейнах свинец представлен в двух формах – в виде
сульфида и в форме растворенного металла. В шлаках свинец обнаружен в форме
оксида, сульфида и растворенного металла. Причем доля оксидной составляющей
свинца в шлаке превалирует. Если исключить механические потери свинца в шлаках
в виде его сульфида, а также долю свинца в виде растворенного металла, то снижения
оксидных потерь свинца в шлаках можно достичь уменьшением концентрации сульфида
свинца в исходном штейне. Это положение полностью подтверждают результаты
практики. Вследствие повышенного содержания в штейнах сульфида свинца и свинца,
растворенного в виде металла свинца, общее содержание последнего в шлаках
остается высоким. Очевидно, что при шахтной сократительной, равно как и при
любой свинцовой плавке на штейн нужно более четко оптимизировать состав
получаемых штейнов с целью обеспечения минимальной растворимости свинца в нем и
снижения содержания его сульфида.
Из вышеизложенного следует, что для
снижения потерь свинца со шлаком необходимо, в первую очередь, минимизировать
долю свинца, растворенного в штейне в виде металла, после чего влиять на
снижение содержания сульфида свинца в штейне.
Литература
1.
Васкевич А. Д., Сорокин М. Л. Модель оксидной растворимости меди в шлаках //
Цветные металлы. 1982. № 7. С. 25-28.
2.
Ванюков А. В., Зайцев В. Я. Шлаки и штейны цветной металлургии. М.:
Металлургия,
1969, с.408.
3.
Володченко С.Н., Васкевич А.Д., Ванюков А.В. Исследование фазовых равновесий в системе Cu – Pb – S при 1473 К. –
РЖ. Металлургия, 1982, №9, реф. 9А91.
4. Манцевич Н.М., Разумовская Н.Н.
Мессбауэровское исследование форм
нахождения железа в шлаках // Цветные
металлы. 1992. № 12. С. 15-19.