ПОЛУЧЕНИЕ
НАНОСТРУКТУР НА ПОВЕРХНОСТИ СИЛИКАГЕЛЯ ПРИ МОДИФИЦИРОВАНИИ ЕГО ХЛОРИДОМ
АЛЮМИНИЯ
Есенаманова Ж.С., Нуркеев
С.С.
Казахский национальный
технический университет имени К.Сатпаева
Для выяснения возможности получения наноструктур на
поверхности силикагеля при модифицировании его хлоридом алюминия вначале были
проведены квантово-химические исследования.
Важной предпосылкой успешного квантово-химического исследования является правильный выбор метода расчёта, прежде всего способа учёта электронной корреляции и применяемого базиса. Первый тест, которому подвергались различные квантово-химические методы – это правильность передачи характера изменения энергии при разрыве связи в различных молекулах. Второй – определение точности передачи геометрической структуры.
Нами, как
наиболее вероятные, рассматривались два пути взаимодействия серы с силикагелем:
замещение гидроксильной группы кремния и внедрение по кислороду гидроксильной
группы.![]()
Для анализа взаимодействия серы с оксидом кремния по этим двум механизмам проводились квантово-химические расчёты с помощью программы Priroda. Оценивались энергия диссоциации и длины Si—S, O—S связей, результаты представлены в таблице 1.
По результатам расчётов связи, образованные одним - двумя атомом серы, являются наиболее прочными. Далее с увеличением атомов серы в цепи энергия связи (Si—S, O—S) уменьшается и стабилизируется. Более прочные связи образуются при присоединении серы по атому кремния (замещение гидроксильной группы).
Таблица 1. Изменение
энергий диссоциации и длин связей при присоединении серы к оксиду кремния
|
Количество
серы в цепочке
|
Присоединение серы по кремнию |
Присоединение серы по кислороду |
||
|
Энергия связи Si—S, кДж/моль |
Длина связи Si—S, пм |
Энергия связи О—S, кДж/моль |
Длина связи О—S, пм |
|
|
S1 |
383,09 |
217 |
290,20 |
171 |
|
S2 |
294,57 |
211 |
253,84 |
172 |
|
S3 |
291,21 |
219 |
247,82 |
172 |
|
S4 |
292,29 |
219 |
238,24 |
172 |
|
S5 |
290,33 |
218 |
236,10 |
171 |
|
S8 |
292,46 |
219 |
236,56 |
171 |
Для определения механизма создания плотной структуры образцов вяжущего с высокими физико-механическими свойствами, были рассмотрены следующие варианты сшивки силикагелевых кластеров. Первоначально, рассматривалась возможность присоединения серного олигомера по механизму, представленному на рисунке 1 (а), когда сера образует прослойки между силикагелевыми кластерами. Оптимизация таких моделей методом функционала плотности (DFT) показала невозможность присоединения с многократным зацеплением серного олигомера вдоль силикагелевого кластера и образование серных прослоек (Рис. 1, б) [1].


а
б
Рис. 1. Механизм присоединения серного олигомера к поверхности силикагелевого кластера: а – начальная геометрия; б – после оптимизации
Далее рассматривалась возможность сшивки силикагеля активными центрами бирадикальной цепи, аналогично сшивке в каучуках, по кремнию (замещение гидроксильной группы) и по кислороду поверхностной гидроксогруппы. Расчеты подтвердили наше предположение и показали, что связи, образованные одним и двумя атомами серы, являются наиболее прочными. Далее с увеличением атомов серы в цепи энергия связи (Si–S, O–S) уменьшается (от 383 кДж/моль до 292 кДж/моль и от 290 кДж/моль до 236 кДж/моль соответственно) и стабилизируется, а длина связи увеличивается (от 217 до 219 пм и от 171 до 172 пм, соответственно). Более прочные связи образуются при присоединении серы к атому кремния. Также был проведен анализ энергии и длин связей внутри серной цепи. При образовании длинных цепочек, в результате взаимодействия серы с поверхностью силикагеля, наблюдается ослабление связей S–S внутри цепи, что говорит о вероятности разрыва этих связей.
Из полученных данных видно, что существует некоторая зависимость прочности связи и длин связей между атомами серы от количества атомов в сульфидной цепи. По данным расчета более прочные связи S–S образуются в молекулах с чётным количеством атомов серы в цепи. Более того, с увеличением атомов серы более трёх наблюдается альтернирование коротких связей, в результате чего формируются дисульфидные "фрагменты" с более прочными и короткими связями. Связь между дисульфидными "фрагментами" несколько "разрыхляется" (энергия связи падает, а длина связи растёт) и при определённых условиях может разорваться. Разрыхление связи в серной цепи ведет к образованию коротких связей, а применение механизма реорганизации (перемешивание) будет способствовать получению плотной структуры за счет отщепления дисульфидных “фрагментов” и плотной пересшивки.
Среди реакций с участием функциональных групп поверхности силикагеля можно выделить реакции нуклеофильного замещения и присоединения. Это реакция с атакой нуклеофильного агента (радикал серы) и нуклеофильное замещение OH–-группы, или нуклеофильного присоединения (внедрение по кислороду).
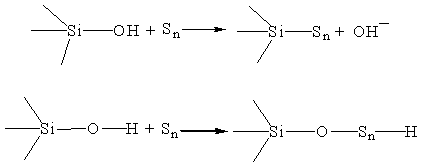
Первоначально оценивалось присоединение одноатомной серы.
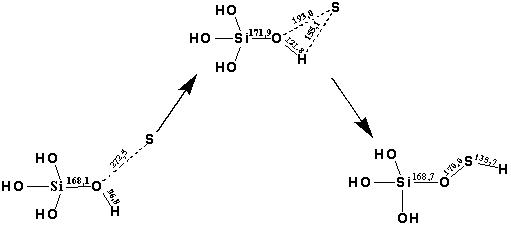
Рис. 2. Схема присоединения серы к поверхности силикагеля – внедрение серы по атому кислорода.
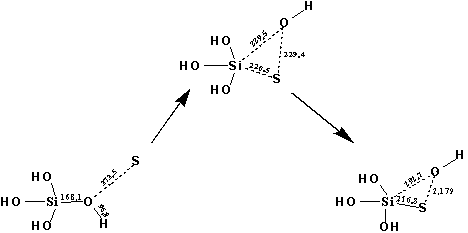
Рис. 3. Схема присоединения серы к поверхности силикагеля – нуклеофильное замещение OH-групп.
По данным метода B3LYP/6-31G(d) реакция внедрения серы по атому кислорода идет экзотермически (-126,78 кДж/моль).
В переходном состоянии (Рис. 2) связь O–H вытягивается до 121,8 пм, а связи O–S и S–H сжимаются и составляют 193,0 и 151,1 пм соответственно. Энергия активации составляет 67,32 кДж/моль.
Реакция присоединения серы к атому кремния с замещениием OH-группы протекает эндотермически (106,86 кДж/моль). В переходном состоянии (Рис. 3) связь Si–O вытягивается до 229,5 пм, а связи O–S и Si–S сжимаются и составляют 229,4 пм и 220,5 пм, соответственно. Энергия активации нуклеофильного замещения составляет 120,16 кДж/моль.
Проведена оценка возможности присоединения серы к модифицированному хлоридом алюминия силикагелю по донорно-акцепторному механизму за счет вакантных d-орбиталей системы силикагель хлорид алюминия и неподеленных электронных пар серного бирадикала.
Полученная нами кривая изменения относительной энергии при сжатии связи S–Al в интервале 500 – 230 пм имеет монотонный характер, что доказывает отсутствие характеристических точек на поверхности потенциальной энергии и барьера реакции присоединения серы к модифицированному силикагелю (Рис. 4).

Рис. 4. Схема присоединения серы к поверхности модифицированного силикагеля.
Как показали результаты наших исследований, наиболее устойчивой является сшивка силикагеля дисульфидными фрагментами. Поэтому наиболее актуальной будет оценка энергии активации аналогичных реакций для двухатомной серы. Был проведен поиск переходного состояния для триплетной и синглетной серы.
Реакция внедрения двухатомной серы (синглет) по атому кислорода идет эндотермически (8,36 кДж/моль). В переходном состоянии связь O–H растягивается до 121,4 пм, а связи O–S и S–H сжимаются и составляют 185,7 и 173,0 пм соответственно. Энергия активации равна 133,76 кДж/моль.
Внедрение триплетной серы идет эндотермически (149,06 кДж/моль). Энергия активации равна 166,91 кДж/моль. Процесс присоединения двухатомной серы (триплет) к атому кремния с замещением OH-группы идет эндотермически (267,02 кДж/моль). В переходном состоянии связь Si–O растягивается до 223,8 пм, а связь Si–S сжимается и составляет 221,0 пм. Энергия активации нуклеофильного замещения составляет 261,33 кДж/моль.
Реакция внедрения синглетной серы по атому кремния идет эндотермически (24,46 кДж/моль). В переходном состоянии связь Si–O растягивается до 189,4 пм, а связи Si–S, S–O укорачиваются и составляют соответственно, 251,5 и 189,6 пм. Энергия активации равна 147,55 кДж/моль.
Термодинамически выгодными с точки зрения энергии активации и наиболее устойчивые соединения будут образовываться в реакции внедрения по кислороду радикалов серы в синглетном состоянии (Еакт=133,76 кДж/моль), а также внедрения радикалов серы в синглетном состоянии по атому кремния (Еакт=147,55 кДж/моль). Продукты этих реакций образуют прочные валентные связи серы с атомом кислорода (280,3 кДж/моль) и атомом кремния (310,4 кДж/мол), определяющие образование прочных СКМ.
Как видно из таблицы 2, внедрение двухатомной серы (М=1) по кислороду и по кремнию энергетически наиболее выгодно. Энергия активации 134 – 148 кДж/моль. Таким образом, прочность композиции достигается за счет реакций внедрения по кислороду и кремнию.
Таблица 2. Энергетическая оценка присоединения серы по различным механизмам.
|
Механизм присоединения серы |
Одноатомная сера |
Двухатомная сера |
|||||
|
∆H (298K) кДж/моль |
Eакт, кДж/моль |
∆H (298K) кДж/моль |
Eакт, кДж/моль |
||||
|
M=1 |
M=3 |
M=1 |
M=3 |
||||
|
Внедрение по атому кислорода |
-126,78 |
67,32 |
8,36 |
149,06 |
133,76 |
166,91 |
|
|
Замещение OH-группы |
106,86 |
120,16 |
24,46 |
261,33* |
147,55 |
267,06* |
|
|
Присоединение к алюминию |
-70,38 |
Нет |
-86,86 |
-8,03 |
Нет |
Нет |
|
*Реакция внедрения по атому кремния.
Присоединение двухатомной серы к модифицированной хлоридом алюминия поверхности силикагеля идет экзотермически (Табл. 2) и безактивационно. Присоединение серы к алюминию, идет по донорно-акцепторному механизму. Длины и энергии связей образующихся соединений представлены на рисунке 5.
. 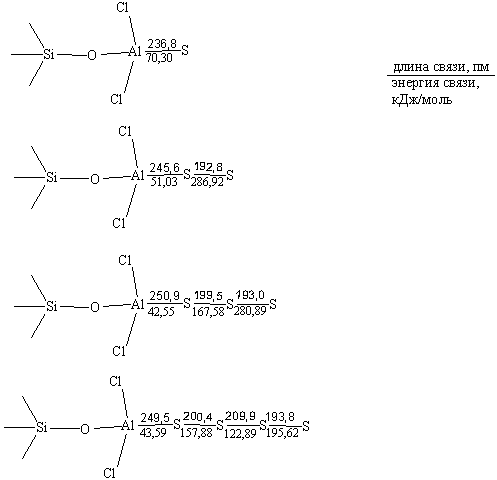
Рис. 5. Схема присоединения серы к модифицированной поверхности хлорида алюминия.
Связь Al–S, образованная одним атомом серы является наиболее прочной. Далее с увеличением атомов серы в цепи она уменьшается и стабилизируется (с 70,30 до 43 кДж/моль), а длина связи увеличивается до 250,9 пм.
При взаимодействии серы с хлоридом алюминия не наблюдается ослабления связи в серной цепи. Непрочные связи серы с алюминием обуславливают перераспределение электронной плотности и упрочнение связей внутри серной цепи.
Хлорид алюминия способствует снижению энергии разрыва серного кольца S4 на 10 кДж/моль. Таким образом, мы можем утверждать, что хлорид алюминия способствует дестабилизации циклов и активирует их разрыв.
Таким образом, модификация силикагеля хлоридом алюминия способствует увеличению активных центров поверхности силикагеля и раскрытию серных колец.
Химическое взаимодействие серы с поверхностью силикагеля по атому кислорода и кремния ведет к созданию монолитного материала обладающего высокой плотностью, прочностью, и устойчивостью к агрессивным средам. Хлорид алюминия, закрепленный на поверхности силикагеля, является катализатором разрыва серных колец.
Таким образом, наше предположение о возможности химического взаимодействия между серой и силикагелем, модифицированным хлоридом алюминия, подтверждается результатами квантово-химических расчетов. При остывании термообработанной смеси активные центры хлорида алюминия будут образовывать слабые донорно-акцепторные связи с не прореагировавшей серой, способствуя ее связыванию и равномерному распределению в пространстве наполнителя [2, 3].
Список использованной литературы
1. Лайков Д.Н. Развитие экономного подхода к
расчету молекул методом функционала плотности и его применение к решению
сложных химических задач.: Дис. Д.Н. Лайкова канд. физ.-мат. наук. Москва. – 2000.
– 102 с.
2. Порфирьева Р.Т., Юсупова А.А., Ахметов Т.Г., Маслий А.Н., Хацринов А.И. Механизм взаимодействия компонентов в композиционных материалах на основе серы и силикагеля // Химия и химическая технология – Иваново, 2004. – т.47 – №2 – с. 37-40.
3.
Герасимов В.В., Ахметов Т.Г., Порфирьева Р.Т., Ахметова Л.Т., Ахмадеев Ф.Г., Габбасов Ф.Г., Юсупова А.А.
Quantum-chemical reseach of sulfur silicagel interaction. / Materials of 16 th
International Congress of Chemical Engineering CHISA-2004, Czech Republic,
Praha, 2004.